人脑胶质瘤皮下成瘤模型
1对1客服专属服务,免费制定检测方案,15分钟极速响应
发布时间:2026-03-06 00:36:57 更新时间:2026-03-05 00:38:59
点击:56
作者:中科光析科学技术研究所检测中心
1对1客服专属服务,免费制定检测方案,15分钟极速响应
发布时间:2026-03-06 00:36:57 更新时间:2026-03-05 00:38:59
点击:56
作者:中科光析科学技术研究所检测中心

人脑胶质瘤皮下成瘤模型构建与应用技术规范
摘要:人脑胶质瘤皮下成瘤模型是神经肿瘤学研究中最常用的体内模型之一,广泛应用于肿瘤生物学机制研究、抗肿瘤药物筛选与评价、以及新型治疗策略的临床前验证。本文系统阐述了该模型的标准化构建流程、多维度检测技术体系、不同研究领域的应用范围、国内外相关检测标准以及核心仪器设备的功能参数,旨在为相关领域研究人员提供全面的技术参考。
1 引言
人脑胶质瘤起源于神经胶质细胞,是最常见的原发性颅内恶性肿瘤,其中以胶质母细胞瘤(GBM)的恶性程度最高,患者中位生存期仅为12-15个月。为深入探究胶质瘤的发病机制及筛选有效治疗药物,建立稳定、可重复的动物模型至关重要。皮下成瘤模型因操作简便、肿瘤生长可直观测量、对动物创伤小等优势,成为胶质瘤研究的基础平台。该模型通过将体外培养的人脑胶质瘤细胞或患者来源的肿瘤组织块(PDX)接种于免疫缺陷小鼠的皮下组织,使肿瘤细胞在活体微环境中增殖形成实体瘤。
2 模型构建流程
2.1 实验动物选择
根据免疫缺陷程度选择适宜的鼠系:
裸鼠(BALB/c-nu):T细胞免疫功能缺陷,适用于大多数胶质瘤细胞系。
NOD-SCID小鼠:T、B细胞联合免疫缺陷,适用于原代细胞或对成瘤率要求高的样本。
NSG小鼠:T、B、NK细胞均缺陷,适用于难成瘤的PDX模型或人源化免疫系统重建研究。
动物周龄通常选择4-6周,体重18-22g,雌雄兼用,但为减少性激素干扰,建议单一性别实验,雌性因性情温顺更常用。
2.2 细胞准备
细胞系来源:U87MG、U251、LN229、A172等经典细胞系,或患者来源的胶质瘤干细胞(GSCs)。
细胞培养:使用含10%胎牛血清的DMEM培养基(干细胞需用无血清培养基加生长因子),在37℃、5% CO₂培养箱中扩增。取对数生长期细胞,胰酶消化后,用PBS或无血清培养基重悬。
细胞悬液制备:调整浓度至1×10⁷ - 5×10⁷ cells/mL,置于冰上备用。为增加初期成瘤率,常与Matrigel基质胶按1:1体积混合(终浓度5×10⁶ - 2.5×10⁷ cells/100μL)。
2.3 接种操作
部位选择:常用双侧或单侧腋窝中后部、腹股沟或背部皮下。腋下因血供丰富,成瘤率最高。
接种方法:75%酒精消毒皮肤,提起皮肤,用1mL注射器(配4号针头)刺入皮下,沿皮下走行约1cm后注入细胞悬液或瘤块,形成皮丘。
接种量:细胞悬液通常100-200μL/点;组织块法将1mm³新鲜肿瘤组织置入穿刺针内推入皮下。
3 检测项目与方法
3.1 肿瘤生长动态监测
原理:通过定期测量肿瘤体积变化,绘制生长曲线,评估肿瘤增殖速度及对干预措施的反应。
方法:接种后3-7天起(依细胞系而定),每2-3天用游标卡尺测量肿瘤长径(L)和短径(W)。体积计算公式:V = (L × W²) / 2 或 V = (π/6) × L × W²。数据以Mean ± SEM表示,绘制时间-体积曲线。
3.2 活体成像检测
生物发光成像(BLI):
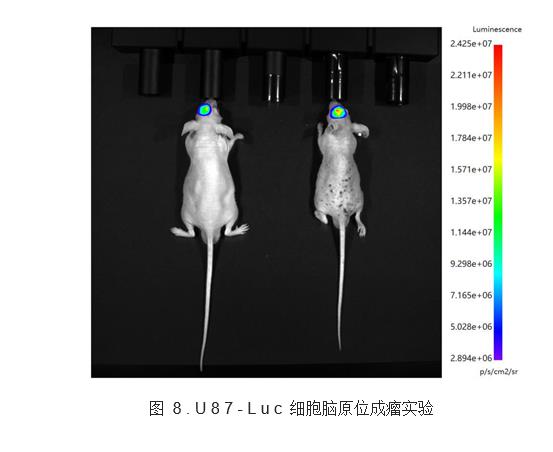
原理:构建稳定表达荧光素酶(Luc)的胶质瘤细胞,接种后腹腔注射底物D-荧光素,在ATP和氧气存在下,荧光素酶催化底物氧化发光,通过高灵敏度CCD相机捕获光子信号。光子通量与活细胞数量呈线性相关。
应用:实现肿瘤早期定植追踪、定量监测肿瘤负荷、评估药物早期疗效。
荧光成像(FLI):
原理:利用GFP/RFP等荧光蛋白标记肿瘤细胞,激发光照射后发射荧光。
局限:组织穿透力较弱,适用于浅表皮下或术中暴露观察。
3.3 超声/光声成像
高频微超声:
原理:40-50MHz高频探头,高分辨率(30-50μm)显示皮下肿瘤边界、内部回声、血流信号。
功能:精确测量体积,评估肿瘤内部坏死、囊变;能量多普勒检测血管生成密度。
光声成像(PAI):
原理:利用脉冲激光照射组织,肿瘤内血红蛋白吸收光能产生热弹性膨胀,发射超声信号。可无创检测血氧饱和度、血红蛋白浓度及肿瘤血管功能。
3.4 组织病理学检测
取材:处死后完整剥离皮下瘤,称重(瘤重是疗效评价的金标准之一),拍照记录大体形态。
包埋切片:4%多聚甲醛固定,石蜡包埋,切取4-5μm厚度切片。
HE染色:
原理:苏木素染细胞核(蓝紫色),伊红染细胞质及细胞外基质(粉红色)。
目的:观察肿瘤细胞形态、核异型性、病理性核分裂象、坏死灶及周边浸润情况。
免疫组织化学(IHC):
原理:基于抗原-抗体特异性结合,通过酶标二抗显色(DAB呈棕黄色),定位和半定量分析特定蛋白表达。
常用指标:
增殖指数:Ki-67(MIB-1抗体),阳性率反映肿瘤增殖活性。
胶质瘤标志物:GFAP(胶质纤维酸性蛋白)、Olig-2、S-100。
干细胞标志:CD133、Nestin。
凋亡检测:Cleaved Caspase-3。
血管生成:CD31或CD34标记微血管密度(MVD)。
免疫荧光(IF):
原理:荧光素标记抗体,在荧光显微镜下共定位检测,常用共聚焦显微镜观察。
3.5 分子生物学检测
Western Blot:
原理:从瘤组织中提取总蛋白,经SDS-PAGE电泳分离,转至PVDF膜,特异性一抗孵育后,酶标二抗结合,ECL化学发光法检测目的蛋白表达量,分析信号通路变化(如PI3K/AKT、MAPK/ERK)。
实时荧光定量PCR(qPCR):
原理:提取肿瘤组织RNA,反转录为cDNA,利用荧光染料(SYBR Green)或探针法(TaqMan)监测PCR进程,检测特定基因mRNA表达水平。
基因测序/组学分析:
原理:提取DNA/RNA进行全外显子测序、转录组测序(RNA-seq),分析模型与原发肿瘤的基因突变谱一致性及药物作用后的基因表达谱变化。
3.6 药物代谢与分布
质谱成像(MSI):
原理:对肿瘤组织切片进行激光解吸电离,通过质谱分析,绘制药物及其代谢物在组织切片上的空间分布图。
高效液相色谱(HPLC)/液质联用(LC-MS):
原理:匀浆肿瘤组织,萃取药物成分,通过色谱分离和质谱检测,定量分析瘤内药物浓度。
4 检测范围与应用领域
4.1 抗肿瘤药物临床前药效学评价
化疗药物敏感性测试:检测替莫唑胺(TMZ)等标准方案对皮下瘤生长的抑制作用。
靶向药物筛选:针对EGFR、VEGF、mTOR等靶点的小分子抑制剂或单克隆抗体药效验证。
新药研发:合成化合物或天然产物的体内抗肿瘤活性筛选。
4.2 新型治疗策略探索
纳米药物递送系统:载药纳米粒、脂质体等在肿瘤部位的富集效率及抑瘤效果。
基因治疗:CRISPR-Cas9基因编辑、溶瘤病毒、siRNA/shRNA递送系统的体内效应。
免疫治疗(需使用人源化免疫系统小鼠):
CAR-T/NK细胞:人源CAR-T细胞对皮下胶质瘤的杀伤作用。
免疫检查点抑制剂:PD-1/PD-L1抗体单独或联合用药疗效。
肿瘤疫苗:负载肿瘤抗原的DC疫苗治疗。
4.3 肿瘤生物学机制研究
癌基因/抑癌基因功能:构建基因敲除或过表达的稳转细胞株,观察皮下成瘤能力及生长速度差异。
肿瘤微环境研究:肿瘤相关成纤维细胞(CAFs)、巨噬细胞(TAMs)在皮下瘤微环境中的作用。
血管生成机制:通过CD31染色、血管灌注实验评估促血管或抗血管生成因子的作用。
4.4 放射生物学研究
放疗增敏剂筛选:联合局部X射线或伽马射线照射,评估药物增加放疗敏感性的作用。
分次照射方案优化:研究不同分割剂量对肿瘤控制率及皮肤放射损伤的影响。
4.5 生物标志物与影像探针开发
分子探针验证:新型PET或荧光探针在皮下瘤模型中的靶向性与成像效果。
液体活检相关:检测荷瘤小鼠外周血中循环肿瘤细胞(CTCs)或外泌体含量与皮下瘤负荷的相关性。
5 检测标准与规范
5.1 国内标准
《实验动物 裸鼠的饲养管理》(GB/T 39650-2020):规定了免疫缺陷动物的环境设施、饲料饮水和微生物控制等级要求(SPF级)。
《抗肿瘤药物药效学评价技术指导原则》(国家药监局,2021年版):明确要求皮下移植瘤模型需详细说明细胞系来源、接种量、动物品系;疗效评价需包含瘤重和瘤体积双指标;规定T/C%(相对肿瘤增殖率)和肿瘤生长延缓天数等评价参数。
《人源肿瘤异种移植模型(PDX)质量控制规范》(中国实验动物学会团体标准 T/CALAS 71-2019):规定了PDX模型的建立、冻存、复苏及传代过程中的质量控制要求,强调遗传稳定性检测(STR鉴定)。
5.2 国际标准
NCI(美国国家癌症研究所)指南:要求皮下瘤模型药效试验至少设3个剂量组,每组8-10只动物;治疗起始体积通常为100-300mm³;评价终点包括肿瘤生长抑制率(TGI)、部分/完全消退率。
OECD(经济合作与发展组织)GLP原则:适用于药物安全性评价研究中的动物实验部分,强调数据可追溯性、SOP操作和环境控制。
美国临床肿瘤学会(ASCO)推荐:在免疫治疗研究中,推荐使用流式细胞术检测肿瘤浸润淋巴细胞(TILs)作为药效辅助指标。
动物实验报告指南(ARRIVE 2.0):要求论文发表时必须详细描述动物种类、品系、性别、周龄、饲养条件、随机化分组方法、盲法测量及统计学处理方法。
6 主要检测仪器设备
6.1 体内成像系统
小动物活体光学成像系统(IVIS):
功能:高灵敏度CCD相机,配备超低温制冷(-90℃),具备生物发光及荧光成像模式。
核心参数:成像视野可调(A-FOV),配备10个以上滤光片(430-850nm),用于多光谱分离,自带Living Image软件用于量化光子通量。
小动物高频超声成像系统(Vevo系列):
功能:实时二维B-mode成像、彩色多普勒、脉冲波Doppler及三维重建。
核心参数:探头频率20-70MHz,轴向分辨率可达30μm,穿透深度10-20mm,适用于皮下及浅表肿瘤微血管血流速度(>1mm/s)检测。
小动物光声成像系统(MSOT/OPO-PAI):
功能:多光谱光声断层成像,可实时检测氧合/脱氧血红蛋白、黑色素、脂质等内源性物质及外源性探针。
核心参数:激发波长680-980nm,空间分辨率150-300μm,成像深度1-3cm。
6.2 病理学分析设备
全自动组织脱水机/包埋机:确保组织处理标准化。
石蜡切片机:精密切片,厚度1-60μm可调,用于高质量组织学切片。
全自动染色机(HE/IHC):实现批量染色标准化。
正置/倒置荧光显微镜:
功能:明场、相差、荧光观察。
核心参数:配备高分辨率彩色/单色CCD,具备电动载物台与Z轴层扫功能。
激光扫描共聚焦显微镜(LSCM):
功能:获取高分辨率光学切片,进行三维重建、共定位分析、荧光共振能量转移(FRET)检测。
核心参数:多通道固体激光器(405、488、561、640nm),超高灵敏度GaAsP检测器,分辨率XY<120nm。
全切片扫描仪(数字病理):
功能:将整个玻璃切片高分辨率数字化,生成全景图像(WSI),便于AI辅助分析、远程会诊及定量分析(如阳性细胞计数、H-Score评分)。
6.3 分子生物学与生化分析设备
实时荧光定量PCR仪:用于基因表达水平绝对/相对定量,具备梯度PCR功能和多重荧光检测能力。
蛋白质印迹系统(电泳+转膜+成像):
化学发光成像仪:CCD冷CCD相机,用于Western Blot ECL发光检测、多色荧光检测及凝胶成像。
流式细胞仪/分选仪:
功能:分析肿瘤组织单细胞悬液中免疫细胞亚群(TILs)、细胞周期、凋亡率(Annexin V/PI染色)、干细胞表面标志。
核心参数:配备多个激光器(例如405nm, 488nm, 640nm),可检测多达10种以上荧光参数。
多功能酶标仪:
功能:MTT/CCK-8细胞活性检测、ELISA(检测小鼠血清中的细胞因子如IL-6、TNF-α)、荧光素酶报告基因检测、药物代谢ADME分析。
6.4 活体给药与局部干预设备
微量注射泵/针泵:用于瘤内精准给药,控制注射速率(μL/h)。
小动物放射治疗系统:
功能:对荷瘤小鼠进行局部精确辐照。
核心参数:X射线能量(如225kV)、剂量率、可调准直器(直径0.5-3cm),配备CBCT(锥形束CT)用于定位和剂量计算。
6.5 常规监测与测量设备
高精度电子游标卡尺:分辨率0.01mm,用于测量肿瘤长径与短径。
电子天平(精密级):量程200g,精度0.1mg,用于称量剥离的瘤重。
小动物麻醉机:异氟烷吸入麻醉,确保成像和给药过程中动物不动且生命体征平稳。
7 数据分析与统计
肿瘤体积数据通常采用重复测量方差分析(Repeated Measures ANOVA)比较不同时间点组间差异。终点瘤重、肺转移结节数等采用单因素方差分析(One-way ANOVA)或非参数检验(Mann-Whitney U检验)。生存分析采用Kaplan-Meier生存曲线及Log-rank检验。p < 0.05 认为具有统计学显著性差异。
8 结语
人脑胶质瘤皮下成瘤模型作为连接体外实验与临床应用的重要桥梁,其技术体系涵盖从动物伦理、精细操作到多模态检测的全流程。随着成像技术的革新(如光声、拉曼成像)和组学技术的融合,该模型已从单纯的生长观察深入到分子事件的可视化与定量化。研究人员在应用该模型时,应严格遵循国家和国际标准,注重实验设计的科学性(如随机、对照、盲法),并结合原位模型、转基因模型等其他模型系统,以获得更全面、更贴近临床实际的研究结论,最终推动胶质瘤诊疗策略的优化与突破。











版权所有:北京中科光析科学技术研究所京ICP备15067471号-33免责声明